对于伴有PFO的缺血性卒中患者,在制定治疗策略之前,需要对PFO与脑卒中的相关程度进行评估,判断PFO是脑卒中的直接病因、危险因素或是偶然发现。概率论表明,在年轻或中年伴有PFO的隐源性脑卒中患者中,73%的脑卒中机制为PFO,27%为其他病因 [4]。与PFO引起脑卒中相关的风险因素有年龄、PFO大小、右向左分流(right-to-left shunt,RLS)程度、PFO形态、ASA的存在、凝血-抗凝系统失衡以及其他心房异常(如右心房间隔囊袋、下腔静脉瓣和希阿里氏网)的共存等 [8]。这些因素可能独立或协同作用,增加栓塞事件的风险。
1.年龄:
研究显示,年轻(年龄截止值为40~60岁)隐源性脑卒中患者的PFO患病率明显高于老年患者(48.9%对27.3%,P<0.000 1)[10]。55岁以上隐源性脑卒中患者与55岁以下患者相比,PFO和隐源性脑卒中之间的相关性强度明显较低[11]。
2.PFO大小:
与其他已知原因的脑卒中患者相比,隐源性脑卒中患者往往有更大的PFO [11]。PFO大小可能是复发性脑血管事件的独立风险因素 [8]。
3.RLS程度:
从右向左流经PFO的流量越大,静脉血栓栓塞穿过心房间分流的机会就越大。研究表明,近70%伴有PFO的不明原因脑卒中患者呈现出较大的RLS,其中超过75%的RLS处于静止状态[12]。另一研究显示与没有隐源性脑卒中的PFO患者相比,有隐源性脑卒中的PFO患者更经常观察到直接RLS(77%对29%,P<0.01)[13]。因此,RLS的检测对识别高风险的PFO可能有潜在价值。然而,RLS程度是动态可变的,可能会因心腔压力、操作者的技术和患者的配合而发生变化,这表明其在临床实践中的可靠性和意义可能有限。
4.ASA:
ASA是否会增加PFO患者脑血管缺血事件的风险仍存在争议。病例对照研究的荟萃分析显示,ASA增加PFO患者脑血管缺血事件的风险( OR=3.69,P<0.010)[11]。然而,随机对照试验的荟萃分析( OR=1.24,P=0.360)以及队列研究的荟萃分析(OR=1.35, P=0.250)均未显示出ASA与PFO患者脑血管缺血事件风险的相关性 [11]。目前关于ASA的前瞻性研究并不全面,伴有ASA和PFO患者的脑卒中复发风险更多体现在部分研究的亚组分析中,且目前仍不清楚ASA通过何种机制影响PFO患者首次和复发性脑卒中的风险。
5.存在或倾向于静脉血栓形成:
由于反常栓塞被认为是PFO相关脑卒中的主要机制之一,因此静脉系统血栓或血栓形成倾向可能对PFO相关栓塞有影响。深静脉血栓形成、盆腔静脉血栓形成和血液高凝状态被认为可能是PFO相关脑卒中的危险因素 [8]。
6.PFO脑卒中风险评估量表:
研究者针对PFO导致脑卒中的相关风险因素进行总结,以量表的方式帮助评估PFO脑卒中的风险。反常栓塞风险(risk of paradoxical embolism,RoPE)量表的组成部分包括年龄、高血压病史、糖尿病史、脑卒中或短暂性脑缺血发作(transient ischemic attack,TIA)病史、是否为吸烟者、影像上是否有皮层梗死6个因素[14]。RoPE量表可以提供PFO与脑卒中相关的概率估计值,评分越高,PFO是脑卒中原因的概率越高[14]。在RoPE量表评分≥7伴有PFO的隐源性脑卒中患者中,估计PFO导致的脑卒中占80%[5]。多中心研究表明RoPE量表有助于识别脑卒中患者的PFO为致病性还是偶发性[15]。然而,RLS程度、ASA和其他PFO高危特征未纳入RoPE量表中,因此,其评估的全面性可能不足。PFO相关脑卒中因果可能性(PFO-associated stroke causal likelihood,PASCAL)分类系统在RoPE量表的基础上进行补充,将RoPE量表与高风险PFO特征(ASA或大量RLS)相结合,将患者分为3类因果关系:不太可能相关、可能相关和很可能相关[16]。有研究者使用经食管超声心动图分析了有脑卒中和无脑卒中PFO患者的PFO形态,根据PFO形态特征区分其致病性或偶然性,并基于此开发了PFO形态学脑卒中因子(morphologic stroke factors of PFO,MorPFO)评分,外部验证显示MorPFO评分表现良好,可能有助于识别高风险的PFO[17]。
目前,PFO相关脑卒中的治疗措施主要包括经导管PFO封堵术和药物治疗,采取PFO封堵术还是单纯药物治疗一直存在着争议[18]。
1.经导管PFO封堵术:
2017年之前的3项随机对照试验(CLOSUREⅠ[19]、PC[20]、RESPECT[21]),结果显示经导管PFO封堵术与单纯药物治疗相比,对于PFO相关脑卒中的二级预防并无优势。在2017年及之后的4项随机对照试验(CLOSE[22]、RESPECT[23]、REDUCE[24]、DEFENSE-PFO[25])则均显示对于PFO相关脑卒中患者经导管PFO封堵术较单纯药物治疗更有效。表1 总结了经导管PFO封堵术与单纯药物治疗有效性及安全性比较的随机对照试验。早期研究与2017年之后研究结果的差异可能是由于早期研究存在以下情况所致:随访时间短(CLOSUREⅠ研究和PC研究均只随访了两年)、未限定PFO脑卒中高危人群,以及封堵器残余分流率(约14%)和封堵器血栓形成率(CLOSURE Ⅰ研究中使用的RESSEAL/STARFlex封堵器器械血栓形成率9%~10%)相对较高[26]。而在CLOSE、RESPECT和REDUCE研究中,手术器械的改进、更严格的入选标准和更长的随访时间则有利于获得PFO封堵术预防脑卒中复发的阳性结果。且这些研究显示无论采用何种药物治疗,PFO封堵术预防脑卒中复发均较单纯药物治疗更有效。随机对照试验参与者个体的荟萃分析表明,单纯药物治疗的患者未来脑卒中复发的年化风险约为1%,而经导管PFO封堵术使该风险降低约60%[16]。基于经导管PFO封堵术有效性的一系列证据,2022年美国心血管造影和介入学会指南强烈推荐18~60岁既往有PFO相关脑卒中的患者使用经导管PFO封堵术,以防止脑卒中复发,且不考虑PFO解剖结构[6]。即高危PFO解剖结构已不作为经导管PFO封堵术的必备条件,低危解剖结构的PFO亦能从中获益。总之,PFO封堵术降低脑卒中复发风险的有效性已获得了随机对照试验较充分的证明,并得到了指南的认可和高级别推荐。
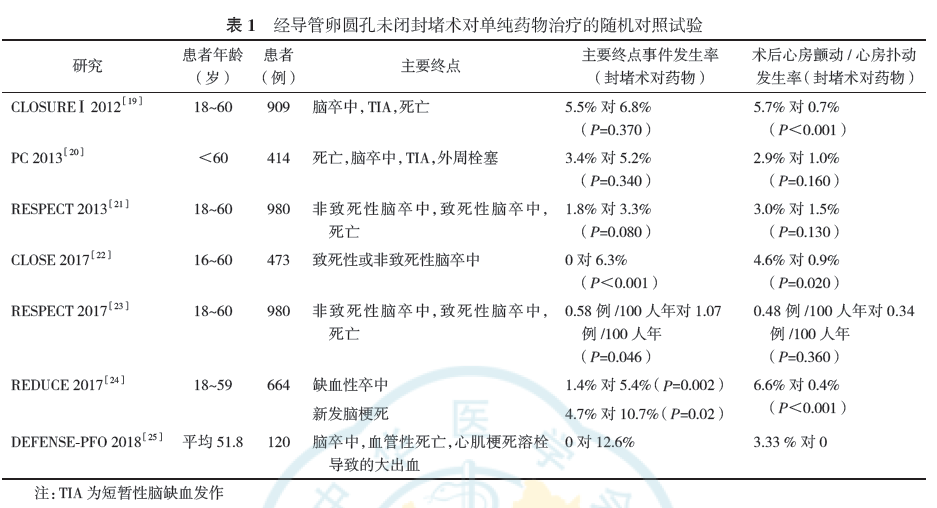
然而,临床试验显示经导管PFO封堵术与较高的器械并发症和房颤发生率相关,房颤风险的增加可能与手术过程中的心房刺激有关[22 ,24]。此外,研究表明,RoPE量表评分较低的患者术后房颤的风险较高,这些患者年龄较大,血管相关脑卒中风险因素较多,而PFO相关脑卒中风险较低,这可能表明隐匿性房颤是这些患者术后房颤的更可能机制,也可能是由于这类患者对器械刺激致心律失常的易感性较高[16]。部分学者认为术后房颤为自限性的,因为在术后发生房颤的患者中,栓塞性卒中的风险没有额外增加[26]。一项队列研究结果显示PFO封堵术的术后房颤风险在长期随访过程中显著降低,PFO封堵术可能不具有发展为长期房颤的风险 [27]。但有研究显示经导管PFO封堵术后28 d内新发房颤、室上性心动过速或房扑的发生率高达20.9%,其中超过80%的患者发生了房颤,显著高于随机对照临床试验中记录的术后房颤发生率[28]。
目前经导管PFO封堵术最佳的获益人群尚不完全清楚,现有随机对照临床试验对PFO高危人群的定义不一致,因此目前最佳受益人群的确定仍存在争议。2022年美国心血管造影和介入学会指南仍然使用RoPE评分≥7分作为推荐标准[6]。有研究将RoPE量表和PASCAL分类系统应用于多项随机试验结果,根据复发性脑卒中的风险降低程度,对可能受益于PFO封堵术的亚组和不太可能受益的亚组进行了区分[16]。未来可能需结合PFO的解剖形态学特征、患者病史、各种诊断技术以及评分系统等进行前瞻性研究以探索更具体的获益人群,进而指导个性化决策。目前试验中的大多数患者≤60岁,因此试验结果可能无法推广到全部人群。有研究显示,经导管PFO封堵术对60岁以上和60岁以下患者可能一样安全有效[29]。另一项研究则显示,>60岁与≤60岁患者相比,经导管PFO封堵术后脑卒中、TIA及外周栓塞的复合发生率较高(P<0.001),且老年患者术后房颤发生率也较高(P<0.001)[30]。需要进一步的前瞻性研究来评估60岁以上患者经导管PFO封堵术的安全性和有效性。
2.药物治疗:
对于老年和不适合或不愿意接受PFO封堵术的年轻PFO相关脑卒中患者,则需要使用药物治疗预防脑卒中复发。PFO相关心源性卒中的血栓来源主要为静脉血栓,因此理论上抗凝相较抗血小板治疗可能对这类患者的治疗获益更大。但抗凝治疗存在出血风险,目前对于这类患者的治疗,抗凝治疗是否比抗血小板治疗更加安全有效尚不明确。目前针对PFO相关脑卒中治疗的指南未推荐抗凝药物优先于抗血小板药物。目前的随机对照试验(PICSS[31]、Shariat等[32]、NAVIGATE ESUS[33]以及RE-SPECT ESUS[34])均未显示合并PFO的脑卒中患者采用抗凝治疗预防脑卒中复发优于抗血小板治疗。表2 总结了PFO相关脑卒中抗凝治疗与抗血小板治疗有效性及安全性比较的随机对照试验。NAVIGATE ESUS研究中PFO患者的亚组分析显示,利伐沙班在降低缺血性卒中复发风险方面优于阿司匹林[35]。RE-SPECT ESUS研究中PFO患者的亚组分析,达比加群酯与阿司匹林在预防复发性脑卒中方面的差异无统计学意义[36]。

然而,荟萃分析的结果与随机对照试验结果有所不同。有随机对照试验的荟萃分析表明,与抗血小板治疗相比,抗凝治疗可能使复发性脑卒中的风险降低约一半[35]。1项前瞻性队列研究显示,对于有PFO的隐源性脑卒中患者,达比加群酯在脑卒中预防方面优于阿司匹林,且达比加群酯不会增加出血并发症的风险[37]。目前尚缺乏关于传统抗凝药与非维生素K拮抗剂口服抗凝药对于PFO相关脑卒中二级预防的前瞻性研究。综合来看,对于PFO相关脑卒中的治疗,目前的证据尚不能说明抗凝治疗优于抗血小板治疗,以及选择何种抗凝药物更安全有效,未来还需要更多证据的验证。
总之,在心源性卒中的中青年患者中PFO检出率远高于正常人群。PFO相关脑卒中的概念被提出并在指南中明确应用。反常栓塞、卵圆孔内原位血栓和房性心律失常是PFO导致脑卒中的可能机制。对于伴有PFO的心源性卒中患者,在制定治疗策略之前,需要对PFO与脑卒中的相关程度进行评估。经导管PFO封堵术的有效性已经过临床试验验证,但研究显示术后房颤发生率较高,且PFO封堵术的最佳获益人群尚不明确。而关于PFO相关脑卒中患者的药物治疗,抗凝治疗是否比抗血小板治疗更加安全有效仍不清楚。